【問題1】
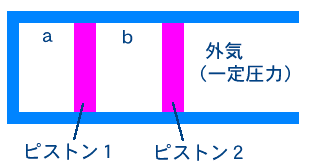
酸素より軽い気体状の炭化水素を用いて燃焼実験を行った。燃焼容器は図に示したように,二つの反応室a,bに分かれている。隔壁(ピストン1,2)はいずれも自由に滑るものとする。実験は反応物質も生成物質もすべて気体で存在する条件で行った。
2種類の炭化水素を混合した気体(混合気体A)に適当量の空気を加えて反応室aに,また2種類の炭化水素を混合した気体(混合気体B)に適当量の空気を加えて反応室bに入れる。温度Tでピストン1とピストン2の位置を測定しておく。
二つの反応室の中に点火火花を飛ばして,炭化水素を完全燃焼させた。反応は爆発的に起こり,ピストンは激しく動くが,やがてある位置に落ち着いて止まった。
反応室a,bの温度をTに戻すと,混合気体Aをつくる2種類の炭化水素の混合比と混合気体Bをつくる2種類の炭化水素の混合比をどのように変えても,ピストン1は反応前の位置に戻ってくることがわかった。混合気体Bをつくる2種類の炭化水素の混合比を変えるとピストン2の戻る位置は変わるが,物質量の比で1:1の場合だけは反応前の位置に戻ってくることがわかった。
下記の問(ア),(イ),(ウ)に答えよ。(イ),(ウ)の解答には途中の式や考え方も簡潔に示せ。なお、気体は理想気体としてよい。必要ならば、原子量はH:1.0,C:12.0,O:16.0を用いよ。
[問]
(ア) 炭化水素CmHnの完全燃焼の化学反応式を記せ。
(イ) 混合気体Aの中にある2種類の炭化水素の化学式を記せ。
(ウ) 混合気体Bの中にある2種類の炭化水素の化学式を記せ。
(東大)
|